오늘(22.4.25.) SK바이오사이언스는 COVID-19 백신 GBP510의 제3상 임상시험 결과를 전자공시를 통해 발표하였다.
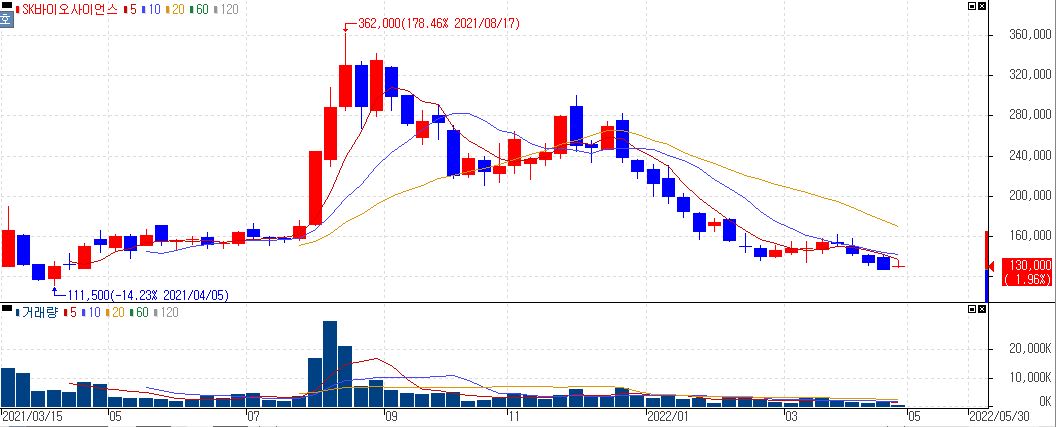
현재 SK바이오사이언스 주가가 고점 대비 많이 밀린 상황이지만, 미래 먹거리 성장산업으로 보고 관심을 가지고 지켜보는 필자로서는 관심이 지대하기에 오늘 포스팅합니다.
참고로, 임상시험 약물이 의약품으로 최종 허가받을 확률은 통계적으로 약 10% 수준으로 알려져 있다고 한다. 임상시험 및 품목 허가 과정에서 기대에 상응하지 못하는 결과가 나올 수 있으며, 이에 따라 당사가 상업화 계획을 변경하거나 포기할 수 있는 가능성도 상존한다고 공시하였다.
주요내용을 살펴보면 아래와 같다.
1. 임상시험 제목
18세 이상의 성인을 대상으로 SARS-CoV-2 재조합 단백질 나노입자 백신(GBP510)의 면역원성 및 안전성을 평가하기 위한 다기관, 평행 비교, 관찰자 눈가림, 활성 대조, 무작위 배정 제3상 임상시험
2. 임상시험 단계 : 제3상 임상 시험
3. 대상질환명 : SARS-CoV-2 감염에 의한 COVID-19 질병 예방
4. 임상시험계획 신청(승인)일 및 승인(시험)기관
- 신청일 : 2021년 6월 28일
- 승인일 : 2021년 8월 10일
- 임상승인기관 : 식품의약품안전처(MFDS)
- 임상시험실시기관 : 고려대학교 구로병원 외 15개 국내 및 해외기관
5. 임상시험 등록번호 : NCT05007951
6. 본 시험은 만 18세 이상 성인을 대상으로 AS03 면역증강제가 포함된 GBP510 백신 25μg의 면역원성 및 안전성을 평가하기 위한 제3상 임상시험으로, 2021년 8월30일 첫 번째 대상자 등록을 시작으로 2022년 1월 14일 총 4,037명 대상자 등록을 완료함. 일차 평가변수로 기초접종(4주 간격 2회 접종) 완료 후 GBP510 백신에 의해 유도되는 중화항체 면역반응의 우위성 및 비열등성을 아스트라제네카사의 COVID-19 백신인 Vaxzevria와 비교 평가하였다고 한다.
7. 임상시험 결과
① 면역원성
- 기초접종 완료 2주 후 GBP510 백신과 Vaxzevria의 중화항체가 기하평균의 비율(GBP510/Vaxzevria)을 통해 우위성 평가기준 상회하여 가설을 만족하였다고 함
- 기초접종 완료 2주 후 GBP510 백신과 Vaxzevria의 항체전환율(접종 전 대비 중화항체가 4배 이상 상승) 차이를 통해 비열등성 여부를 평가한 결과, 비열등성 허용한계 상회하여 가설을 만족하였다고 함
② 안전성
- 현재 분석 진행 중으로 추후 공시 예정이라고 한다.
8. 기대효과
GBP510 기초접종 후 면역가교(Immunobridging) 기준을 모두 만족하는 높은 예방효과와 동등 혹은 그 이상의 백신유효성을 추정할 수 있다고 한다.
9. 향후 계획
안전성 결과 추가 확보하여 성인에서 GBP510 백신 기초접종 후 COVID-19 질병 예방 적응증에 대한 국내 및 해외 허가신청을 진행할 예정이라고 한다.
※ SK바이오사이언스(302440)
[2021년도 말 기준]
- 자산총계 : 2조1,101억 원
- 부채총계 : 5,088억 원
- 자본금 : 382억 원
- 자본총계 : 1조6,013억 원
- 매출액 : 9,290억 원
- 영업이익 : 4,742억 원
- 당기순이익 : 3,551억 원
- 주당 순이익 : 4,844원
[참고자료]
- 전자공시시스템 DART
- 한국투자증권
- 미래에셋증권
'2. 경제 잔치마당 > 경제정보' 카테고리의 다른 글
| [주식] 삼성전자 1분기 실적 발표 (1) | 2022.04.28 |
|---|---|
| [주식] 분기배당주(삼성전자,POSCO,신한지주, KB금융 등) (0) | 2022.04.26 |
| [주식] SK바이오사이언스의 실적 및 배당금 (1) | 2022.03.28 |
| [주식] 대신증권 실적 및 배당금과 자사주 취득 (7) | 2022.03.15 |
| [주식용어] 서킷브레이커와 사이드카 (4) | 2022.03.15 |




댓글